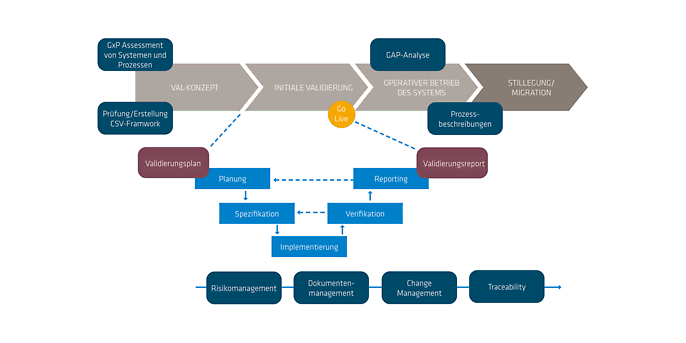
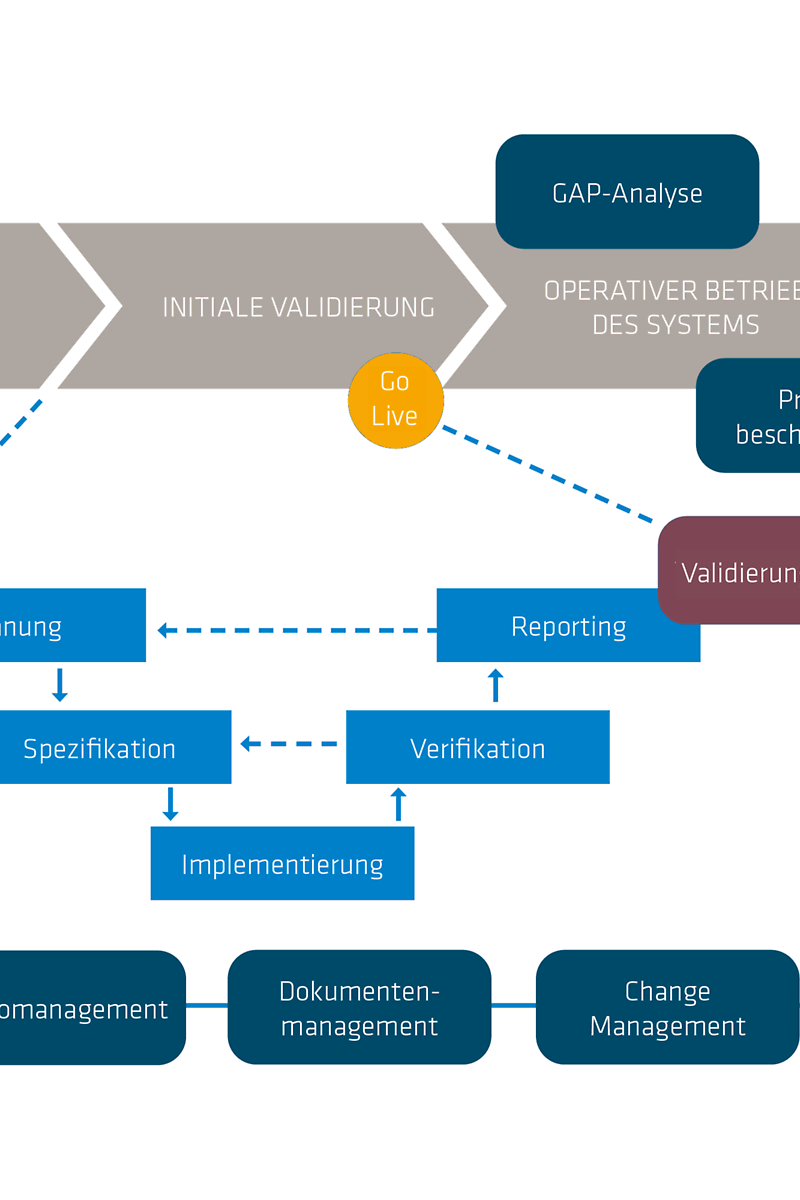
Im GxP-Umfeld ist die Softwareentwicklung und -einführung stark reguliert, um in den unterstützten Geschäftsprozessen die Patientensicherheit, Produktqualität und Datenintegrität sicherzustellen. Jeder Softwarefehler kann hier Menschenleben gefährden. Eine der regulatorischen Kernanforderungen ist die Validierung von computergestützten Systemen. Mit der sogenannten Computer-System-Validierung (CSV) wird der dokumentierte Nachweis geliefert, dass das entsprechende computergestützte System seinen beabsichtigten Nutzen stets und in gleichbleibender Qualität erfüllt. Dabei greifen Standards der Softwareentwicklung aus dem GAMP5 sowie weitere Vorgaben wie zum Beispiel 21 CFR Part 11 oder EU Annex 11.
Mit adesso haben Sie die richtigen Fachleute an Bord
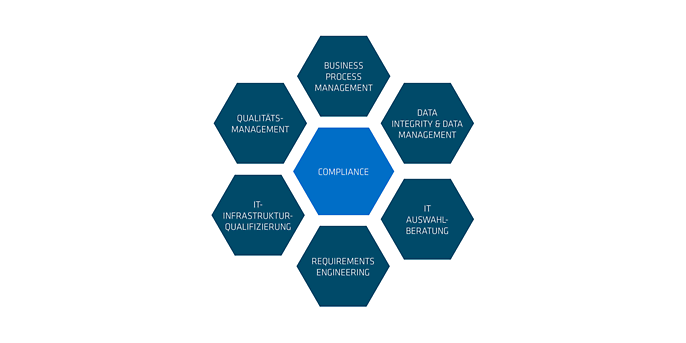
Unser Life-Sciences-Bereich besteht aus Fachleuten, die langjährige CSV-Erfahrung mit dem entsprechenden Branchen-, Technologie- und Prozess-Know-how vereinen. Gepaart mit exzellenten Kommunikations- und Moderationsskills verstehen unsere Consultants es bestens, zwischen allen Stakeholdern zu vermitteln, die IT- und Businessbereiche zusammenzubringen und gemeinsam die passenden Strategien und Prozesse zu entwickeln.
adesso verfolgt dabei einen pragmatischen Validierungsansatz, der zwischen den regulatorischen Anforderungen und der IT ausgleicht. Sie und Ihr Team erhalten von uns eine maßgeschneiderte Validierungslösung, um GxP-Compliance zu erreichen und aufrechtzuerhalten: von der Validierungsstrategie bis zur Ausführung der Validierungsaktivitäten – inklusive der vollständigen Validierungsdokumentation. Das Ganze unabhängig davon, um welches Computersystem es sich handelt.